PD-1抗体如何拓展抗病毒治疗新 frontier?
原创PD-1抗体如何拓展抗病毒治疗新 frontier?
原创
STARTER
发布于 2026-03-12 09:21:14
发布于 2026-03-12 09:21:14
一、PD-1抗体在肿瘤治疗中为何备受瞩目?
PD-1抗体作为免疫检查点抑制剂的代表,正在深刻改变肿瘤治疗格局。其作用机制是通过阻断PD-1与PD-L1的结合,解除肿瘤细胞对T细胞的免疫抑制,重新激活机体自身的抗肿瘤免疫应答。目前,PD-1抗体已在黑色素瘤、非小细胞肺癌、头颈癌、肾细胞癌、霍奇金淋巴瘤、膀胱癌、结直肠癌及胃癌等多种恶性肿瘤中显示出显著疗效,成为肿瘤免疫治疗的核心药物之一。然而,近年来的研究发现,PD-1抗体的应用潜力远不止于肿瘤领域,其在艾滋病(HIV)等病毒感染性疾病中的探索同样引人关注。
二、PD-1与HIV潜伏感染有何关联?
HIV感染的核心难题在于潜伏病毒储存库的存在。抗逆转录病毒治疗(ART)可有效抑制病毒复制,但无法清除整合入宿主基因组的潜伏前病毒。这些潜伏感染的CD4+ T细胞不产生病毒蛋白,因而逃避免疫系统识别及药物杀伤,成为实现功能性治愈的根本障碍。
研究表明,HIV感染者的CD4+ T细胞表面PD-1表达水平显著升高,且与患者病毒载量及CD4计数密切相关。PD-1作为免疫抑制分子,不仅介导T细胞耗竭,还参与维持HIV潜伏状态。在潜伏感染的细胞中,PD-1信号通路抑制病毒基因转录,使病毒保持沉默状态。因此,PD-1成为连接免疫耗竭与病毒潜伏的关键分子节点。
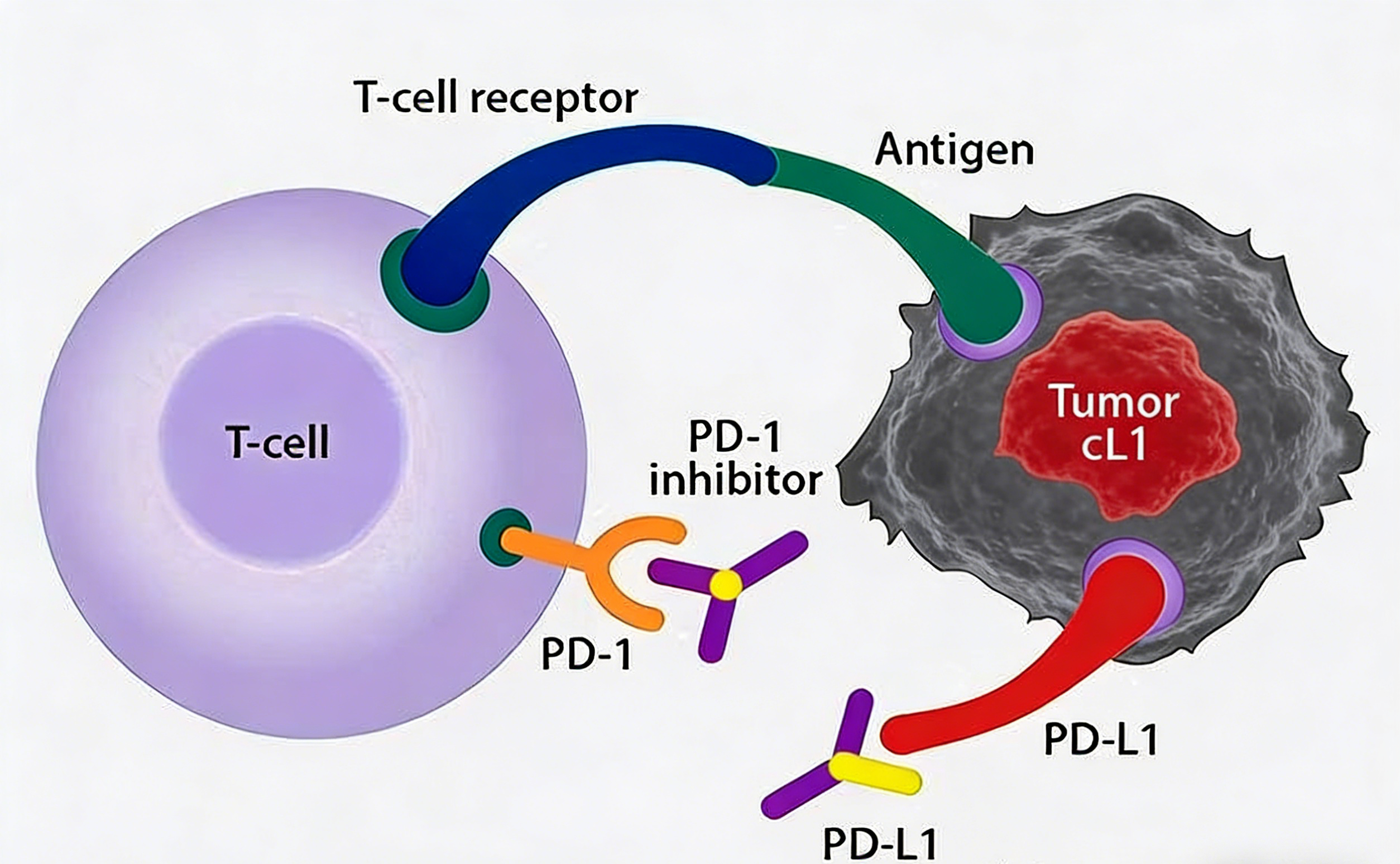
三、PD-1抗体如何影响HIV潜伏储存库?
基础研究揭示,PD-1抗体可通过双重机制干预HIV潜伏感染。一方面,PD-1抗体阻断抑制性信号,可直接逆转潜伏感染细胞中PD-1介导的转录沉默,促使潜伏病毒苏醒。在体外实验中,PD-1抗体联合潜伏逆转剂(如HDAC抑制剂)可显著增加HIV的再激活效率,提示其在“休克-杀灭”(Shock and Kill)策略中的潜在价值。
另一方面,PD-1抗体可恢复耗竭T细胞的效应功能。苏醒后的病毒表达病毒抗原,激活的HIV特异性CD8+ T细胞可识别并清除病毒复制活跃的感染细胞。这一过程同时作用于潜伏储存库的激活与清除,为实现储存库耗竭提供了可能。
四、临床病例为PD-1抗艾提供了哪些证据?
临床观察为PD-1抗体的抗HIV潜力提供了初步证据。在一例肺癌合并HIV感染的病例中,患者接受PD-1抗体(帕博利珠单抗)治疗后,肿瘤得到有效控制的同时,其HIV感染相关指标亦发生显著变化。治疗初期,原本检测不到的HIV病毒血症出现短暂反弹,提示潜伏储存库被激活;随后病毒载量持续下降,CD8+ T细胞活性显著增强,表明抗病毒免疫应答得到恢复。更重要的是,治疗120天后,HIV储存库呈现持续而显著的下降。
这一案例虽为孤例,但揭示了PD-1抗体同时作用于肿瘤与HIV的独特价值。病毒血症的短暂反弹证实了潜伏激活效应,其后储存库的下降则提示免疫清除功能恢复。尽管无法排除个体差异及合并治疗影响,该结果为PD-1抗体用于HIV功能性治愈提供了临床概念验证。
五、PD-1抗体抗HIV的潜在机制是什么?
PD-1抗体抗HIV的潜在机制可归纳为三层级。第一层级直接作用于潜伏感染细胞:PD-1抗体阻断PD-1信号后,解除对HIV转录的抑制,促使潜伏病毒苏醒,使储存库细胞转化为病毒复制活跃状态。
第二层级作用于耗竭T细胞:PD-1抗体恢复HIV特异性CD8+ T细胞的增殖能力及效应功能(如IFN-γ、TNF-α分泌),使其能够有效识别并清除病毒复制的感染细胞,重建抗病毒免疫监控。
第三层级作用于储存库动态平衡:通过持续激活与清除的双重作用,逐步耗竭潜伏储存库,减少病毒反弹的潜在来源。这一机制与“休克-杀灭”策略高度契合,为HIV功能性治愈提供了新思路。
六、PD-1抗体抗艾面临哪些挑战?
尽管前景可期,PD-1抗体用于HIV治疗仍面临多重挑战。安全性是首要考量。PD-1抗体激活免疫系统可能诱发免疫相关不良事件(如肺炎、结肠炎),在HIV感染者中需权衡获益与风险。此外,潜伏激活可能导致的病毒血症反弹是否可控,尚需更多研究验证。
疗效不确定性同样值得关注。单一病例的成功无法推广至所有HIV感染者。病毒储存库的大小、分布及异质性可能影响治疗反应;PD-1表达水平、免疫耗竭程度及宿主遗传背景亦可能造成个体差异。联合治疗策略需系统优化,包括与抗逆转录病毒药物的时序配合、与潜伏逆转剂的协同应用等。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读

