汉堡大学 BioChemAIgent AI 全程自动化:小分子分析 + 蛋白建模 + 分子对接 + 可视化全覆盖!
汉堡大学 BioChemAIgent AI 全程自动化:小分子分析 + 蛋白建模 + 分子对接 + 可视化全覆盖!

DrugIntel
发布于 2025-12-30 20:17:37
发布于 2025-12-30 20:17:37

在基于结构药物发现领域,AI技术的突破已成为加速研发进程的核心动力,但现有计算工具的碎片化、高专业化门槛等问题,仍制约着其在产业界和学术界的规模化应用。德国汉堡大学医学中心等机构联合研发的BioChemAIgent框架,以智能体架构为核心,整合顶尖AI模型与经典计算化学工具,构建了覆盖小分子分析、蛋白建模、分子对接及相互作用解析的端到端解决方案,为该领域带来了兼具专业性与易用性的技术革新。本文将从技术架构、核心功能、性能验证及应用价值等维度,对这一创新框架进行深度拆解。
一、技术背景:结构基药物发现的痛点与AI agent的破局之道
基于结构药物发现的核心逻辑是基于生物靶点(主要为蛋白质)的三维结构,设计或筛选能与之特异性结合的小分子化合物,其关键环节包括靶点结构解析、小分子性质评估、分子对接预测及结合机制分析。然而,传统研发模式面临三大核心痛点:
- 工具碎片化:蛋白结构预测、小分子预处理、分子对接等环节依赖不同的专业工具(如AlphaFold用于结构预测、AutoDock Vina用于对接),需手动整合流程,效率低下且易引入人为误差;
- 专业门槛极高:各工具的参数设置、格式转换、结果解读均需深厚的结构生物学与计算化学知识,限制了非专业研究者的使用;
- 可重复性不足:缺乏标准化的工作流记录与执行规范,不同团队的实验结果难以复现与对比。
近年来,大语言模型(LLMs)与智能体(Agent)技术的兴起为解决上述问题提供了新思路。Agent具备自主规划任务、选择工具、协调执行的能力,而BioChemAIgent正是基于这一理念,通过Model Context Protocol(MCP)实现AI模型与专业工具的深度协同,其核心创新在于:以统一接口封装多样化工具,以透明化推理替代黑箱操作,以社区化架构支撑持续迭代,最终实现 专家级流程自动化 。
二、核心架构:三层协同设计,构建全流程技术底座
BioChemAIgent的架构设计遵循 客户端-服务器-工具链 三层协同模式,确保了系统的灵活性、扩展性与易用性,具体如下:
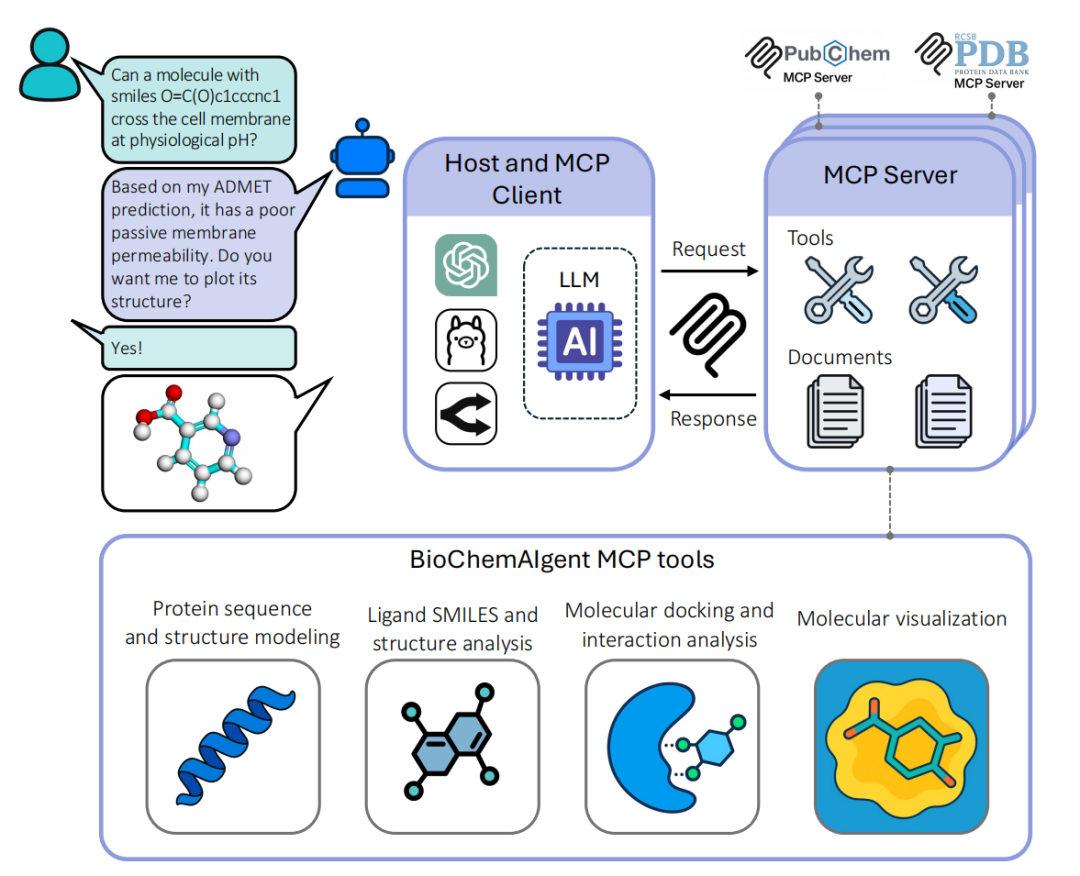
图1. BioChemAIgent的整体架构。BioChemAIgent包含一个客户端、多个服务器和一个用户界面(UI)聊天机器人。该客户端遵循模型上下文协议(MCP),可由OpenAI、Ollama或OpenRouter托管的大语言模型(LLM)驱动。系统集成了三个MCP服务器:PubChem-MCP-Server、PDB-MCP-Server以及一个定制的BioChemAIgent-MCP-Server。该定制服务器配备了用于蛋白质序列与结构预测分析、配体SMILES及结构处理、分子对接与相互作用分析以及分子可视化的工具。该服务器还附有指导智能体遵循最佳实践使用这些工具的文档。一个在线用户界面可公开访问,同时提供对话式聊天机器人和分子结构查看器功能。
1. 客户端层:多LLM适配的智能交互核心
客户端采用MCP协议,支持集成OpenAI、Ollama、OpenRouter等平台的LLM模型,用户可根据需求选择不同算力与成本的方案(如Ollama的gpt-oss:120bcloud为免费选项)。其核心功能包括:
- 自然语言解析:将用户的药物研发需求(如 将布洛芬与Cox-1蛋白对接 )转化为可执行的技术任务;
- 工作流规划:基于工具能力与任务目标,生成标准化的执行路线图(如 靶点结构获取→蛋白预处理→小分子优化→分子对接→结果分析 );
- 工具调用协调:自动调用服务器端工具,处理格式转换、参数传递等底层逻辑,并将结果反馈给LLM进行自然语言解读。
2. 服务器层:三大MCP服务器的功能协同
系统整合了三类MCP服务器,形成覆盖数据检索、核心分析与可视化的完整支撑体系:
- PubChem-MCP-Server:对接ChEMBL等化学数据库,提供小分子化合物的结构数据、理化性质等基础信息检索;
- PDB-MCP-Server:连接RCSB PDB数据库,支持实验测定的蛋白结构下载,为后续分析提供靶点基础;
- BioChemAIgent-MCP-Server:核心功能服务器,集成27款专用工具(基于19个软件包开发),覆盖小分子分析、蛋白建模、分子对接、相互作用分析及可视化五大模块,是全流程执行的核心引擎。
3. 工具链层:专业化工具的模块化封装
工具链是BioChemAIgent的核心竞争力,其特点是 精选工具+标准化接口 。研发团队筛选了结构生物学与计算化学领域的主流工具,并通过统一的Python字典格式实现输出标准化,确保工具间的无缝衔接。工具链可分为四大核心模块:
模块 | 核心工具 | 核心功能 |
|---|---|---|
小分子分析 | OpenBabel、RDKit、ADMET-AI | SMILES与3D结构互转、能量最小化、质子化、立体异构体生成、ADMET参数预测 |
蛋白建模 | ESM3、AlphaFold3、FoldX | 蛋白序列补全、3D结构预测(单体/多聚体)、结构修复、质子化与能量优化 |
分子对接 | AutoDock Vina、Smina、Gnina、DiffDock、AlphaFold3 | 基于物理与深度学习对接方法全覆盖,支持盲对接与靶向对接,自动计算结合亲和力 |
可视化与交互分析 | py3Dmol、Plotly、PLIP | 蛋白-小分子复合物3D渲染、结合位点高亮、氢键/离子键等相互作用可视化 |
三、核心功能:四大关键环节的技术突破与应用场景
BioChemAIgent的核心价值在于将结构基药物发现的关键环节实现自动化与标准化,以下对各模块的技术细节与应用场景进行深度解析:
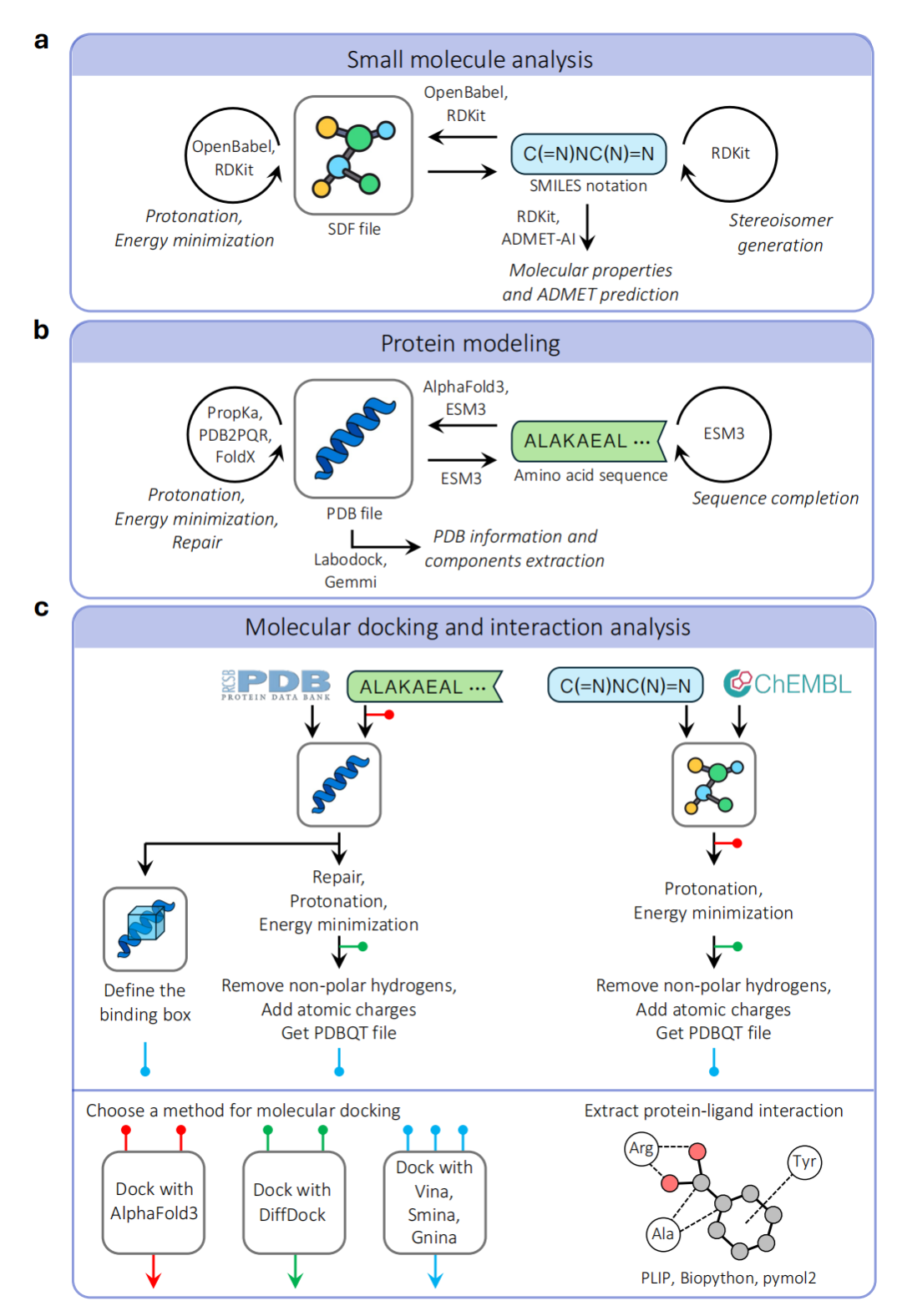
图2. BioChemAIgent工作流程示意图。(a)小分子分析:分析配体SMILES、由结构数据文件(SDF)提供的三维结构,并实现两者间的相互转换。(b)蛋白质建模:分析蛋白质序列、由蛋白质数据库(PDB)文件提供的蛋白质结构,并实现两者间的相互转换。(c)分子对接与相互作用分析:包括蛋白质和配体的预处理、使用不同方法(如Vina、Smina、Gnina、DiffDock和AlphaFold 3)进行对接,以及蛋白质-配体相互作用分析。
1. 小分子分析:从结构表征到成药潜力评估的一体化解决方案
小分子的结构与理化性质直接决定其成药潜力,该模块的核心优势在于 全维度表征+自动化预处理 :
- 结构转换与优化:支持SMILES(如布洛芬的SMILES:CC(C)CC1=CC=C(C=C1)C(C)C(=O)O)与SDF/PDB格式的双向转换,通过OpenBabel实现能量最小化与指定pH条件下的质子化(如生理pH=7.2),确保结构的合理性;
- 异构体制备:基于RDKit自动生成立体异构体与互变异构体,解决小分子结构的多态性问题;
- 成药性质预测:整合RDKit与ADMET-AI工具,计算分子量、LogP(脂水分配系数)、TPSA(拓扑极性表面积)等关键参数,预测吸收、分布、代谢、排泄、毒性(ADMET)特征,快速筛选出具有成药潜力的化合物。
2. 蛋白建模:AI驱动的靶点结构精准构建与优化
蛋白质结构的准确性是分子对接成功的前提,该模块整合了当前最先进的AI建模技术:
- 结构获取双路径:对于有实验结构的蛋白,直接从PDB数据库下载;对于无实验结构或结构不完整的靶点,通过ESM3与AlphaFold3实现高精度预测——ESM3擅长序列补全与功能预测,AlphaFold3则支持蛋白-核酸、蛋白-小分子复合物的结构预测,二者协同确保靶点结构的完整性与准确性;
- 结构预处理自动化:通过PropKa计算pKa值并优化质子化状态,利用FoldX修复 torsion角异常、范德华冲突等结构缺陷,通过PDB2PQR进行能量优化,为分子对接提供“即插即用”的高质量靶点结构。
3. 分子对接:多方法融合的结合模式精准预测
分子对接是评估小分子与靶点结合能力的核心环节,BioChemAIgent的创新在于 方法全覆盖+流程标准化 :
- 多方法协同选择:整合基于物理(AutoDock Vina、Smina、Gnina)与基于深度学习(DiffDock、AlphaFold3)两类对接方法,系统可根据靶点类型(如单体蛋白、复合物)、输入数据(如仅序列或有结构)自动选择最优方案——例如,仅提供蛋白序列时,优先使用AlphaFold3直接预测蛋白-小分子复合物结构;
- 标准化预处理流程:自动完成小分子与蛋白的预处理(去除非极性氢、添加原子电荷、定义对接网格),其中对接网格可基于共结晶配体坐标自动生成,避免手动设置的主观性;
- 结合亲和力与相互作用解析:通过经验评分函数(如Vina评分)估算结合亲和力,利用PLIP、Biopython等工具提取氢键、疏水作用、离子键、π-π堆积等关键相互作用,为化合物优化提供明确方向。
4. 可视化模块:零代码实现专业级结构解读
结构可视化是结果分析与学术展示的关键,但传统工具(如PyMOL)需手动编写脚本。BioChemAIgent推出两款核心可视化工具:
- render_structures:基于py3Dmol封装,支持SDF/PDB文件的3D渲染,可自定义原子样式、表面规则,高亮对接网格与结合位点,用户通过自然语言即可调整可视化参数(如 突出显示Arg120与布洛芬的离子键 );
- interaction_plot:专注于蛋白-小分子相互作用的直观展示,以图形化方式标注各类结合力的位置与强度,降低结果解读的专业门槛。
三、性能验证:双重评估体系,彰显专家级可靠性
为验证BioChemAIgent的性能,研发团队设计了 LLM自动评估+专家人工评估 的双重体系,覆盖准确性、鲁棒性与实用性三大维度:
1. LLM自动评估:鲁棒性与准确性的规模化验证
- 评估设计:构建13组覆盖全功能模块的“问题-标准答案”对,通过GPT-5生成5种语义重构或语法拼写错误的查询变体(如故意写错分子SMILES符号),测试10种不同LLM驱动下系统的响应效果;
- 核心结果:GPT-5驱动的BioChemAIgent表现最佳,工具调用准确率98.5%、任务解读准确率100%、结果呈现准确率96.0%,即使面对严重 错误 的查询,仍能准确恢复核心需求并输出正确结果,彰显了极强的鲁棒性。
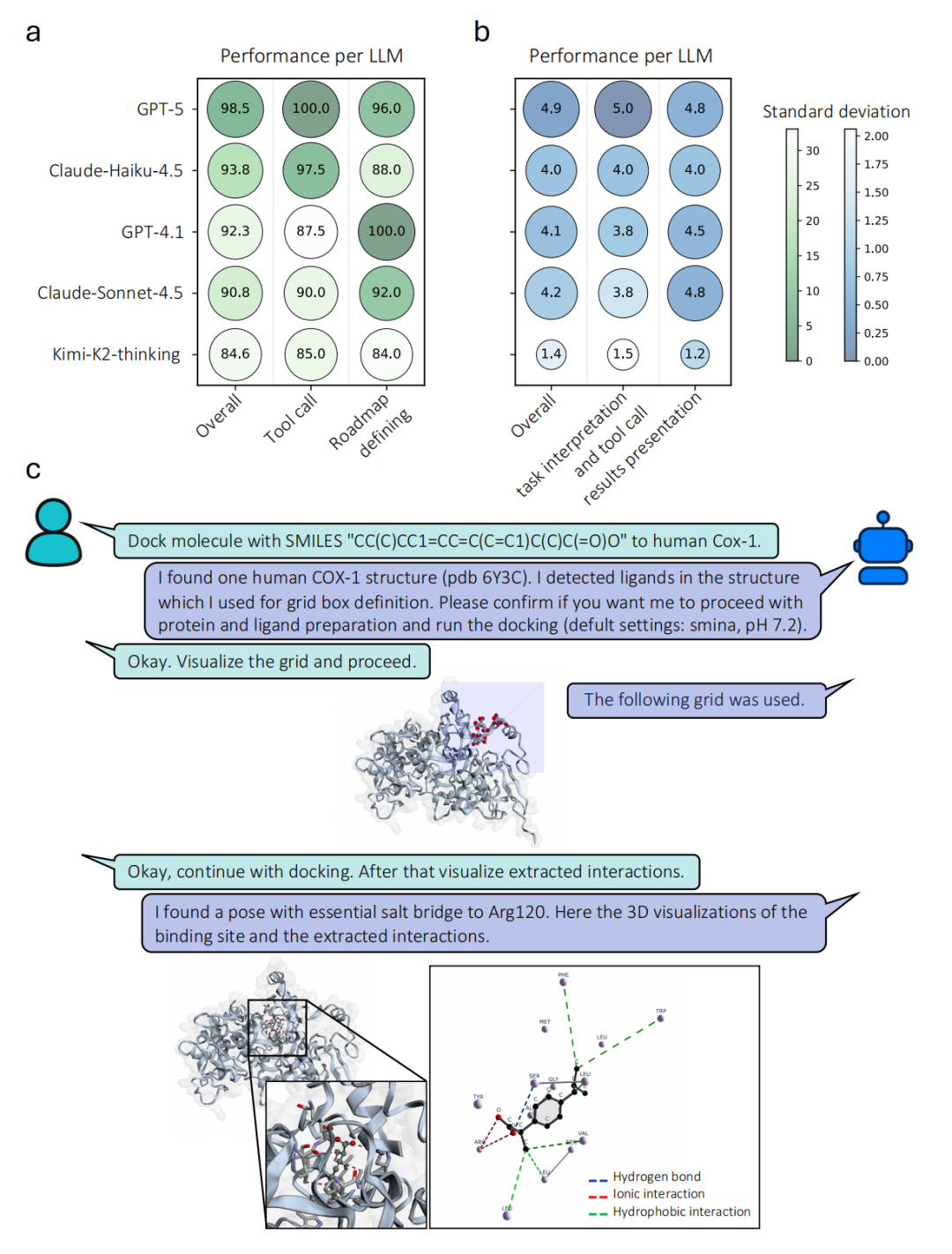
图3. BioChemAIgent的评估与演示。(a)基于大语言模型(LLM)的自动评估与(b)基于专家的人工评估在不同LLM间的性能比较。点的大小和颜色深度表示各任务得分的平均值和标准差。(c)用户与智能体就Cox-1与布洛芬分子对接任务进行对话的简化示意图。
2. 专家人工评估:复杂场景下的实用性验证
- 评估设计:由领域专家设计4个真实药物研发场景(如 未知结构靶点的小分子筛选、蛋白-小分子结合机制解析),从 工具选择正确性、结果解读准确性、流程透明性和结果呈现精度四个维度进行0-5分评分;
- 核心结果:GPT-5驱动的系统在所有场景中平均得分4.8分(满分5分),尤其在 隐式任务推理 (如用户未明确指定预处理步骤,系统自动补全流程)中表现突出,其分析逻辑与结果质量达到领域专家水平,证明系统并非简单的工具调用,而是具备深度的领域知识与推理能力。
3. 典型案例:布洛芬与Cox-1蛋白的对接验证
为直观展示系统性能,研发团队以 布洛芬与人类Cox-1蛋白对接 为案例进行验证:
- 靶点获取:系统自动从UniProt检索Cox-1蛋白信息,匹配到唯一对应的PDB结构(6Y3C);
- 预处理:自动提取蛋白链、去除溶剂分子,基于共结晶配体坐标定义对接网格,同时完成布洛芬的质子化(pH=7.2)与能量最小化;
- 进行对接:默认选择Smina工具执行对接,成功识别出布洛芬与Cox-1蛋白Arg120残基的关键离子键相互作用(这一机制已被生物学实验证实);
- 结果可视化:自动生成3D结构模型,高亮结合位点与相互作用类型,实现 从需求到结论 的全流程自动化,整个过程无需用户干预工具操作。
四、总结
BioChemAIgent的推出,不仅整合了当前药物研发领域的顶尖工具和AI模型,更通过agent架构实现了 工具协同+智能推理 的深度融合。它将原本分散、复杂的计算药物研发流程整合为一站式解决方案,既降低了专业门槛,又提升了研究的效率和可重复性。
赶紧访问项目官网体验,或通过GitHub获取源码,让AI为你的药物研发工作赋能吧!
相关资源获取
- 开源代码仓库:https://github.com/imsb-uke/bcai
- 在线Web界面(含聊天机器人与分子可视化工具):https://bcai.ims.bio
- 预印本原文:https://doi.org/10.64898/2025.12.17.694892
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-12-20,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

