Nat. Commun. | Flexynesis:面向精准肿瘤学的多组学深度学习整合工具包
Nat. Commun. | Flexynesis:面向精准肿瘤学的多组学深度学习整合工具包

DrugAI
发布于 2026-01-06 12:41:10
发布于 2026-01-06 12:41:10
DRUGONE
精准肿瘤学中的决策依赖于多模态分子信息的整合,但现有大多数基于深度学习的多组学整合方法缺乏透明性、模块化和可部署性,且通常局限于狭窄的任务范围。研究人员提出了 Flexynesis,一个端到端的深度学习工具包,支持数据预处理、特征选择、超参数优化和标记物发现。用户可在统一的接口下选择深度学习架构或经典机器学习方法,执行回归、分类和生存分析等任务,既可单任务训练,也支持多任务建模。研究人员展示了 Flexynesis 在药物反应预测、癌症亚型建模和生存分析等多种场景中的应用潜力。该工具已通过 PyPI、Guix、Bioconda 和 Galaxy Server 提供,降低了临床和前临床研究中使用深度学习整合多组学数据的门槛,使缺乏深度学习经验的研究者也能便捷使用。

癌症是一类复杂疾病,其发生与基因组异常紧密相关,涉及细胞死亡抵抗、免疫逃逸、组织侵袭及持续增殖信号等多种特征。与罕见单基因疾病不同,癌症等复杂疾病需要理解多个细胞调控层之间的交互关系,因此需要跨转录组、表观组、蛋白质组、基因组、代谢组和微生物组等层面的多组学整合。
目前,已有多项国际计划构建了大规模多组学数据库(如 TCGA、CCLE),为癌症及其他复杂疾病研究提供了丰富的分子数据。然而,现有的多组学整合工具存在诸多限制:
- 缺乏可复用性和适配性,很多研究仅提供零散脚本,难以在不同场景中复现;
- 缺少标准化操作流程,例如数据清理、特征选择与超参数优化;
- 功能局限,往往仅支持分类、回归或生存建模中的单一任务;
- 在某些场景下,经典机器学习(如 SVM、随机森林)甚至优于深度学习,但缺乏统一平台进行系统比较。
针对这些问题,研究人员开发了 Flexynesis ——一个灵活、模块化且可扩展的工具包,能够系统化支持多组学整合任务。
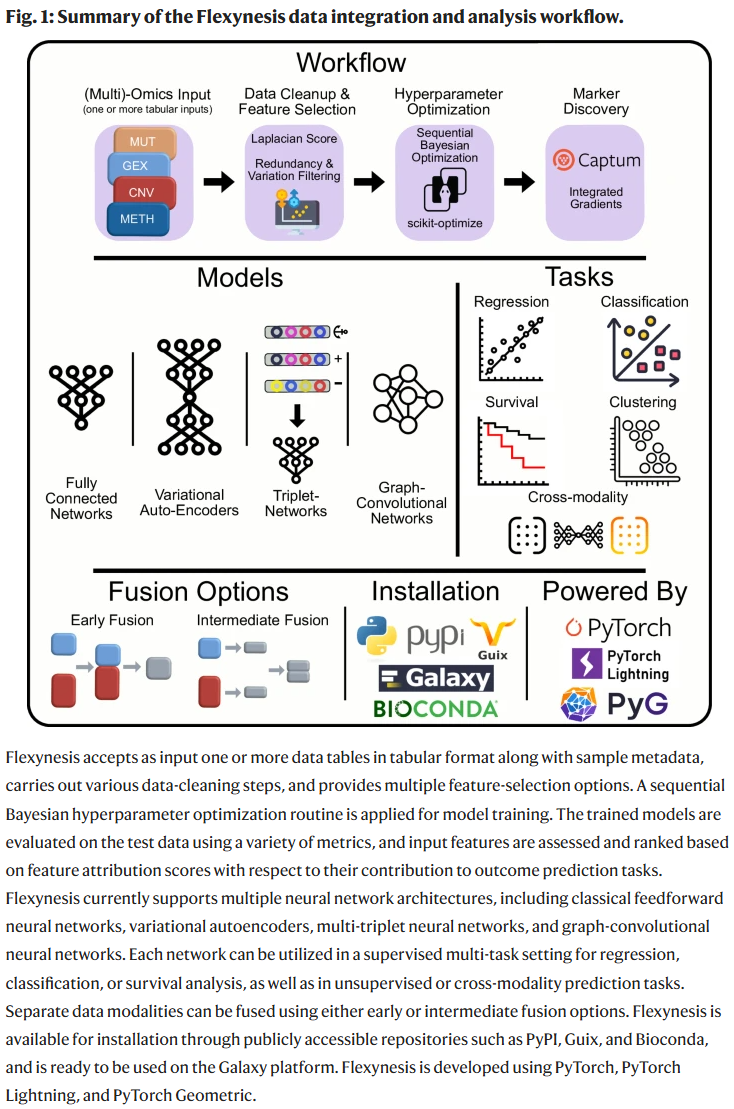
结果
单任务建模
研究人员展示了 Flexynesis 在三类任务上的应用:
- 药物反应预测(回归):利用 CCLE 数据训练模型,预测拉帕替尼和塞卢美替尼的药物敏感性,在独立的 GDSC 数据集中取得了高度一致的预测效果。
- 癌症亚型分类:在多个 TCGA 队列中,Flexynesis 使用基因表达和甲基化数据高精度预测微卫星不稳定性(MSI)状态,即使不依赖突变数据,AUC 仍达 0.98。
- 生存分析:在低级别胶质瘤(LGG)与胶质母细胞瘤(GBM)患者数据上,模型基于 Cox 损失函数预测生存风险,结果显示高低风险组在 Kaplan-Meier 生存曲线上显著分离。
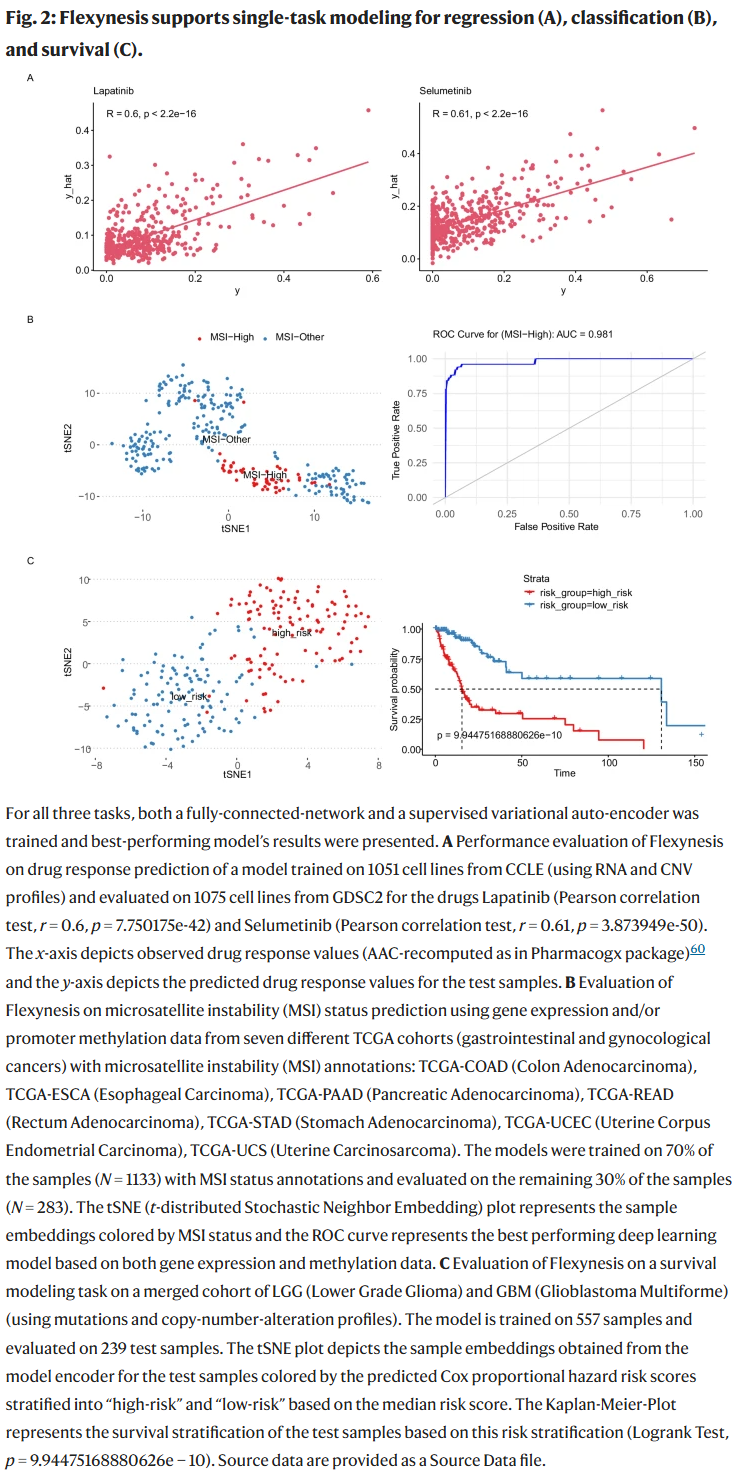
多任务建模
Flexynesis 支持同时预测多个临床变量。在转移性乳腺癌队列(METABRIC)中,研究人员分别建立了:
- 仅预测亚型标签的模型;
- 仅预测化疗状态的模型;
- 同时预测亚型与化疗状态的多任务模型。
结果显示,多任务模型能够在同一嵌入空间中清晰区分两个变量,提高了对临床特征的整体表征能力。
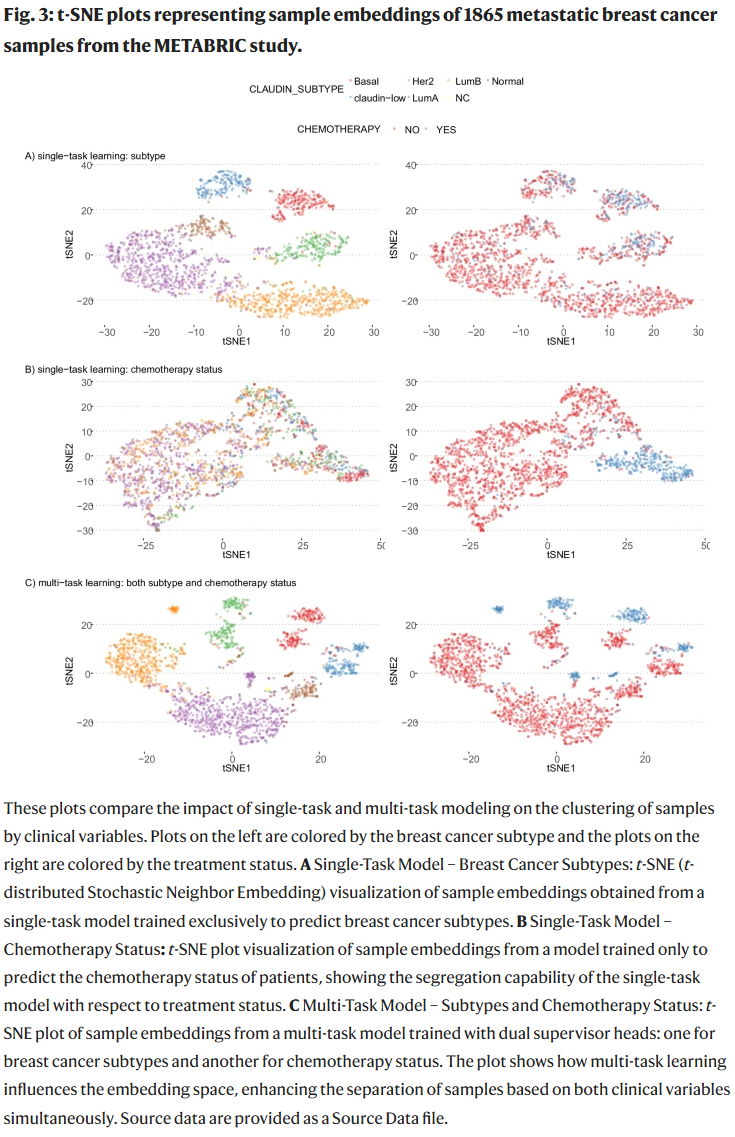
同时处理多个临床变量
在 LGG 与 GBM 队列中,研究人员同时预测年龄、组织学亚型和生存结局,模型嵌入结果能够层次化地反映三者关系,并识别出共同关键基因(如 IDH1、EGFR 等),验证了 Flexynesis 在多变量综合预测中的价值。
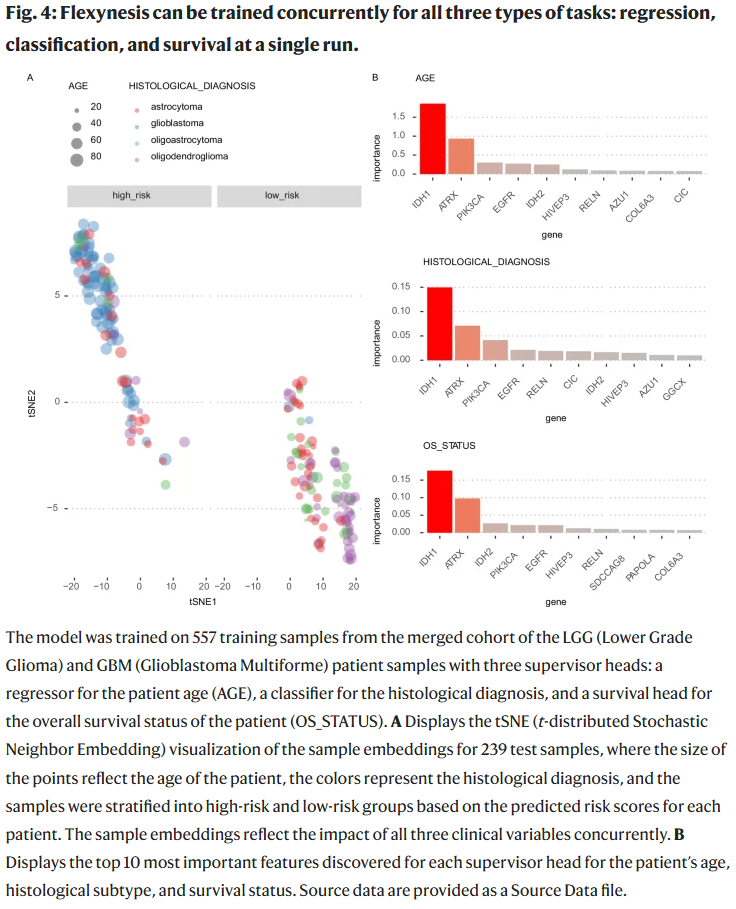
无监督与跨模态学习
Flexynesis 还支持无监督学习与跨模态预测:
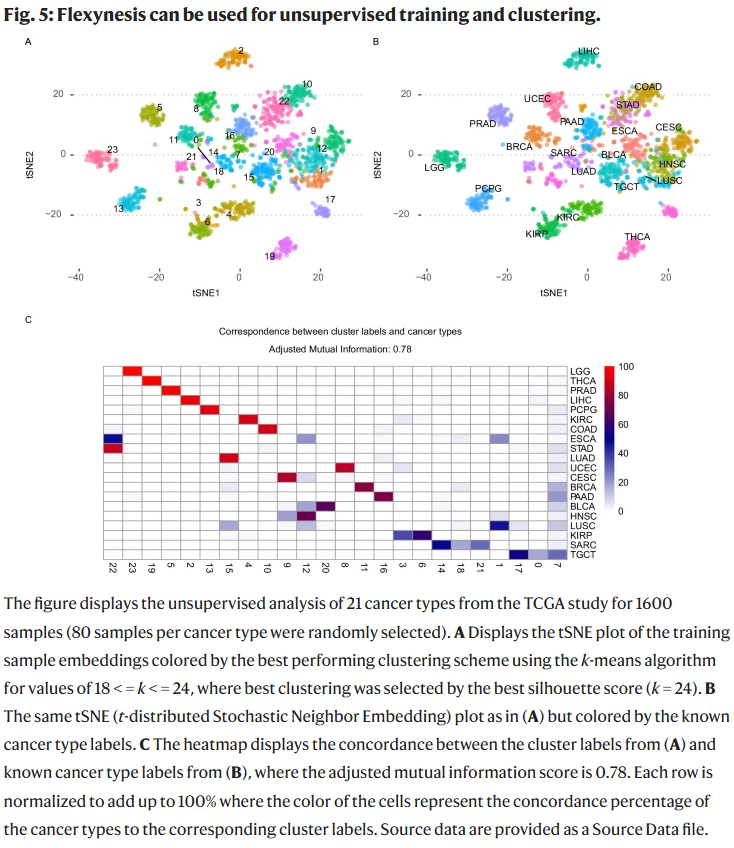
- 无监督聚类:在 21 种癌症类型的 TCGA 数据中,Flexynesis 成功区分不同癌症类型,调整互信息分数达 0.78。
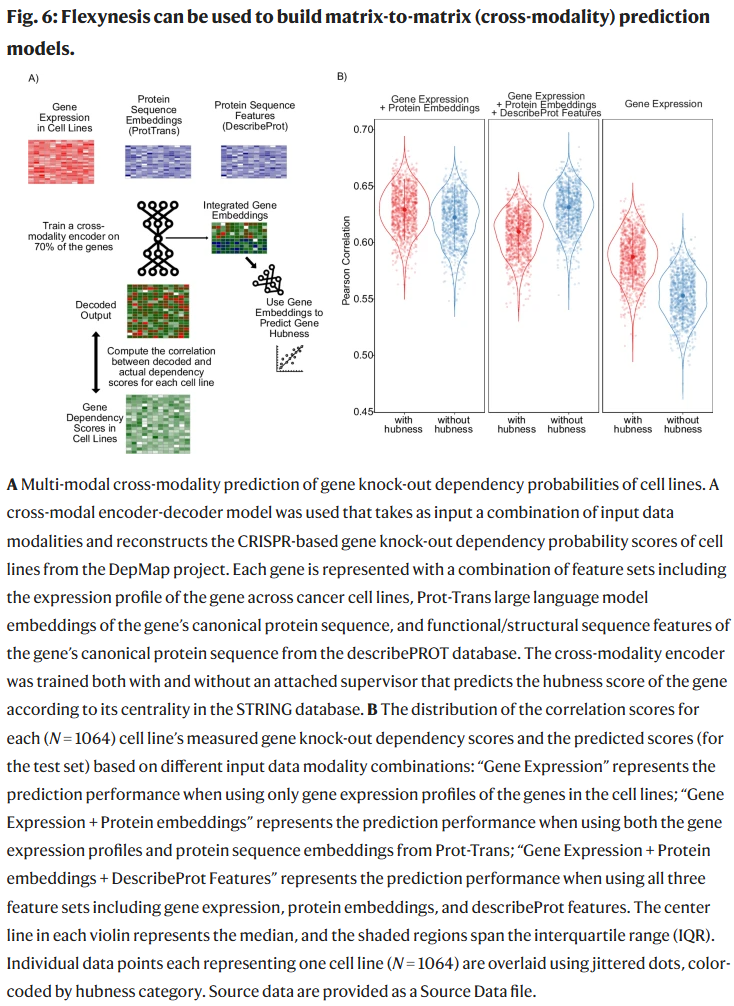
- 跨模态预测:利用 DepMap 数据,Flexynesis 将基因表达与蛋白序列嵌入结合,预测基因敲除依赖性得分,性能优于单一模态输入。
模型微调与药物反应标记物发现
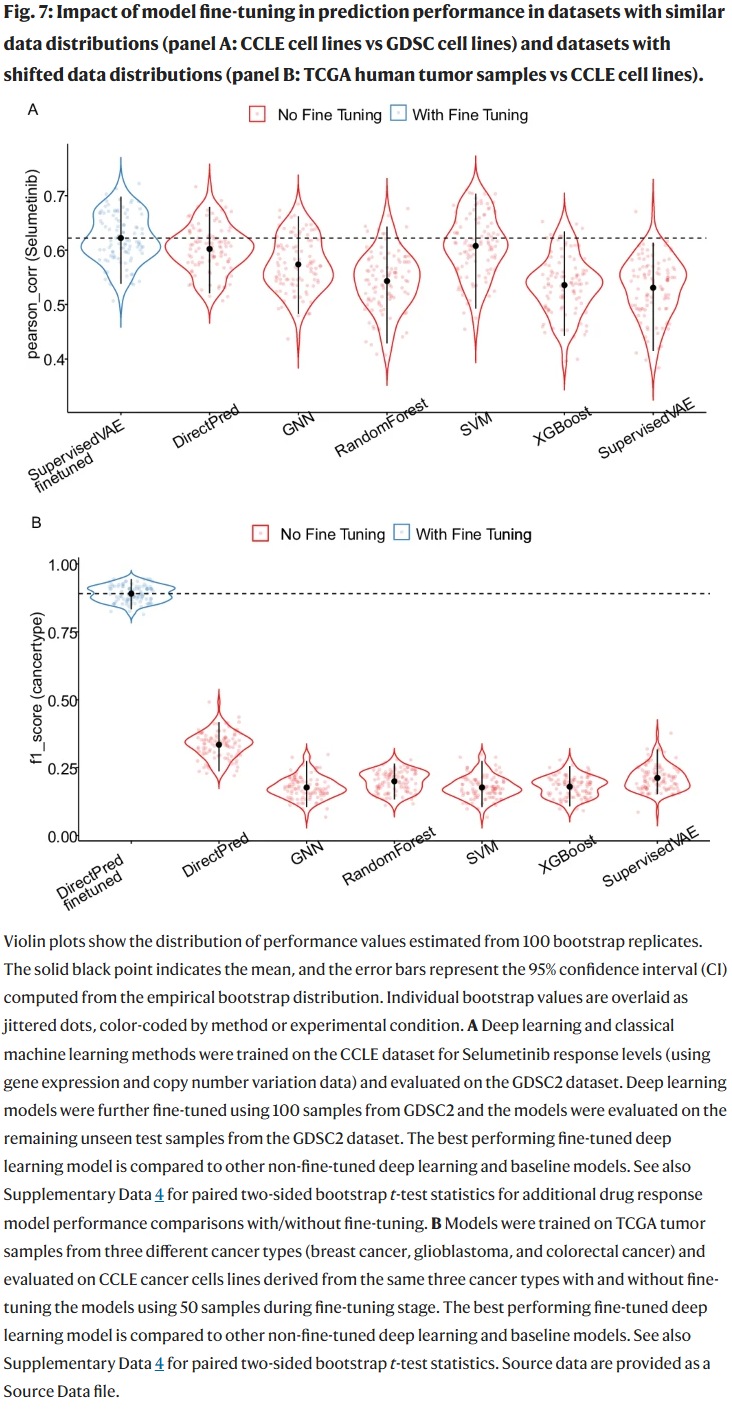
研究人员表明,Flexynesis 可通过小样本微调显著提升跨队列预测性能。例如,在 TCGA 肿瘤样本到 CCLE 细胞系的迁移任务中,F1 分数由 0.16 提升至 0.8。
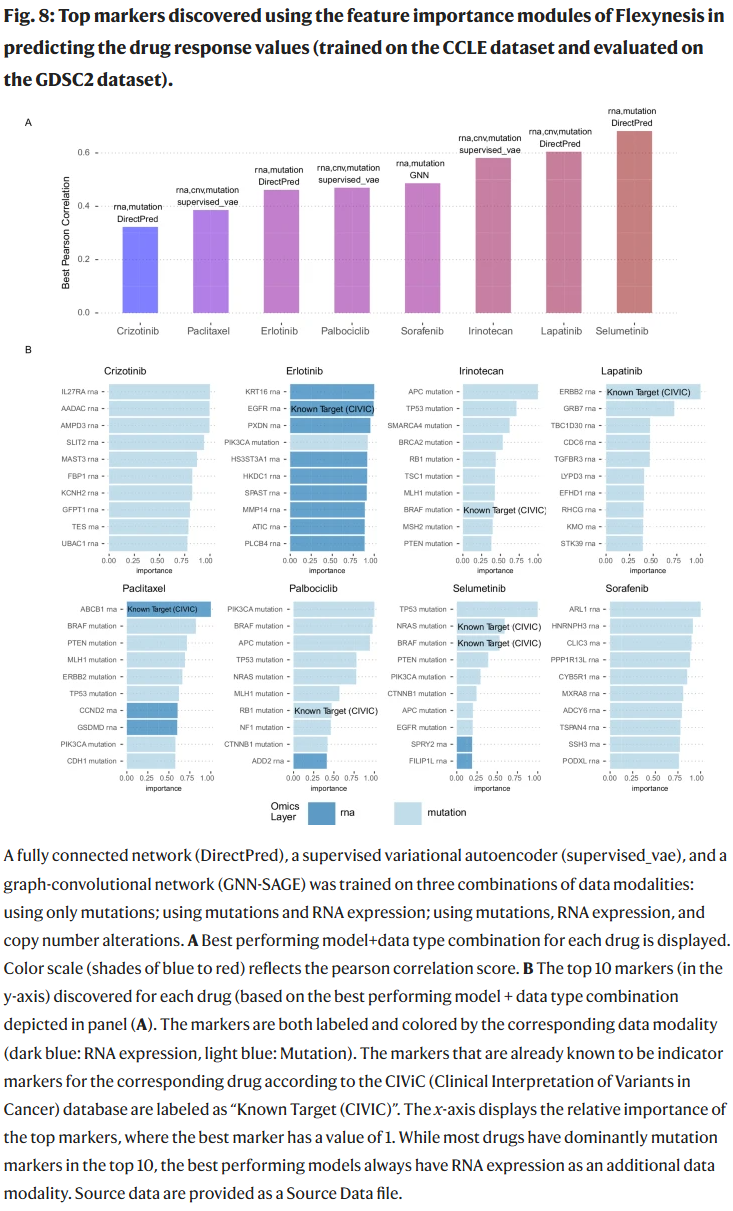
此外,Flexynesis 内置标记物发现模块,能够识别与药物反应相关的基因标记物。对于 8 种药物中的 6 种,模型成功捕捉到已知的临床可操作标记物,同时强调 RNA 表达与突变联合使用能显著提高预测性能。
系统化基准测试
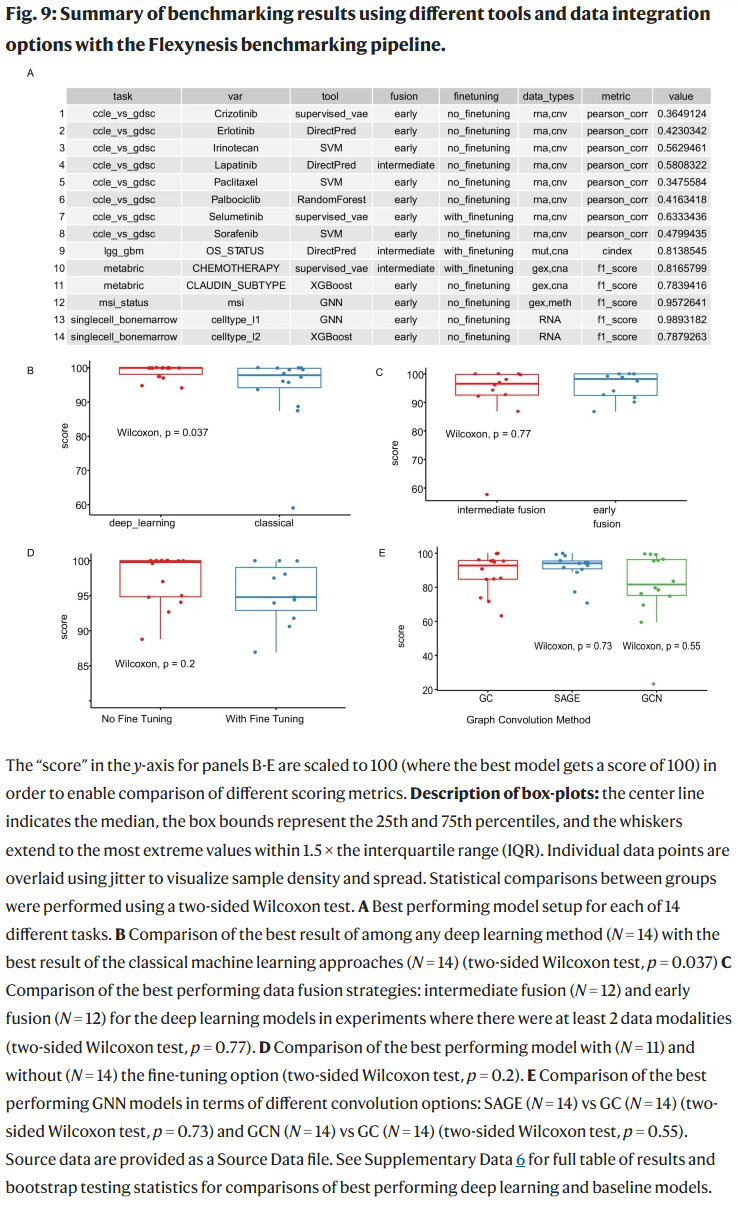
研究人员设计了 14 个任务、222 个实验,比较不同模型架构、融合方式和调优策略。结果显示:
- 深度学习与经典方法性能相近,具体选择取决于任务;
- 不同融合策略(早期/中期)差异不显著;
- 微调在数据分布差异较大时更具优势;
- 在图神经网络中,SAGE 卷积方法略优于其他选项。
讨论
研究人员提出的 Flexynesis 并非全新的深度学习算法,而是一个将多种现有组件整合到统一框架中的工具包,核心贡献在于:
- 用户体验提升 ——标准化数据清理、特征选择、超参数优化与模型评估流程。
- 灵活性与适配性 ——支持多模态输入、多任务建模、监督与无监督学习、跨模态预测。
- 普适性 ——不仅适用于多组学数据,还可处理其他表格型数据。
- 可及性 ——开源发布,提供文档、示例数据和基准测试管道,方便研究人员快速上手。
虽然深度学习在部分场景中未必优于经典方法,但其在处理多任务、缺失标签、跨模态学习和迁移学习中的优势,使其在临床多组学研究中具备广阔前景。随着多组学测序成本下降与规模提升,Flexynesis 将进一步推动精准肿瘤学与复杂疾病研究的发展。
整理 | DrugOne团队
参考资料
Uyar, B., Savchyn, T., Naghsh Nilchi, A. et al. Flexynesis: A deep learning toolkit for bulk multi-omics data integration for precision oncology and beyond. Nat Commun 16, 8261 (2025).
https://doi.org/10.1038/s41467-025-63688-5
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-09-14,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

