Nat. Biotechnol. | AI加速抗体筛选:高效发现具备类药物特性的高质量结合分子
Nat. Biotechnol. | AI加速抗体筛选:高效发现具备类药物特性的高质量结合分子

DrugAI
发布于 2026-03-30 18:46:37
发布于 2026-03-30 18:46:37
DRUGONE
近年来,多家AI生物技术初创公司不断展示由人工智能辅助完成的抗体发现成果,并宣称该技术具有改变行业格局的潜力。然而,大多数核心模型仍未公开,缺乏统一基准测试,使得外界难以全面评估这些突破的真实水平。尽管如此,计算机设计抗体正迅速成为生物药研发领域最受关注的方向之一。

2024年11月,David Baker团队在University of Washington发表了一篇具有里程碑意义的Nature论文,首次系统描述了利用机器学习从头设计抗体结合分子的过程。这项研究证明,人工智能不仅可以预测蛋白结构,还能够直接生成针对特定靶点的抗体序列。AI公司Xaira的首席技术官Hetu Kamichetty指出,这是首篇经同行评审验证的“从零开始抗体设计”研究。Xaira由Baker实验室成员联合创立,融资规模达到10亿美元,目前正开发具有类药物性质的AI设计抗体,并计划推进人体临床研究。
传统抗体发现流程通常需要长达两年时间,才能将一个初始命中分子优化为可进入临床开发阶段的候选药物。通过展示技术或小鼠免疫获得的抗体,往往需要进一步进行亲和力成熟和可开发性优化,包括稳定性、溶解性、药代动力学、药效学以及免疫原性等指标。研发人员通常通过逐个替换氨基酸来改善这些属性,但这种方法十分耗时,而且某一属性的改进往往会牺牲另一属性的表现。
生成式人工智能被认为有望改变这一局面。通过在设计阶段同时优化多个可开发性指标,AI模型可以显著缩短研发周期,并节省数百万美元成本。更重要的是,它可能使研究人员能够针对传统方法难以处理的靶点设计抗体,例如多跨膜蛋白或高度动态的受体蛋白。
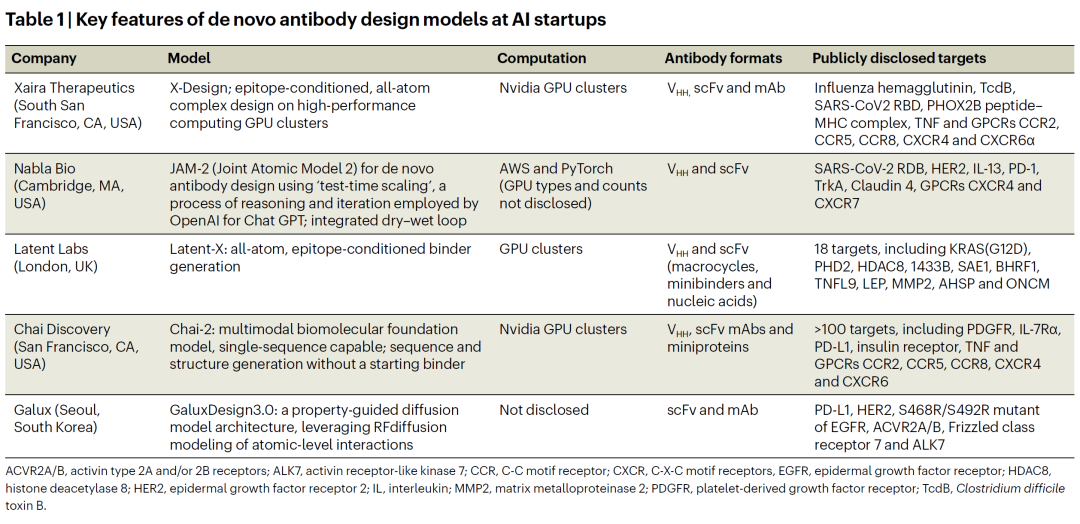
在2025年初的J.P. Morgan医疗健康大会前后,多家大型制药公司相继宣布与AI抗体设计公司建立合作。Eli Lilly与Chai Discovery和Isomorphic Labs达成合作;Sanofi和Pfizer分别与Earendil Labs和Boltz建立合作关系。2024年11月,Chai完成1.3亿美元融资,并公布其Chai-2模型,据称可从头设计完整单克隆抗体,成功率超过50%,比早期方法提升两个数量级。最新结果显示,该模型甚至可以针对G蛋白偶联受体(GPCR)和MHC复合物等困难靶点生成高亲和力抗体。
与此同时,伦敦的Latent Labs宣布,其Latent-X2模型在预测纳米抗体和scFv结构时成功率约为50%,并能针对KRAS(G12D)等传统上难以成药的靶点设计皮摩尔级亲和力抗体。公司还报告其从头设计的抗体在人体T细胞实验中几乎不产生免疫原性。
另一家公司Nabla Bio开发的JAM-2模型可成功设计针对GPCR CXCR7的抗体,并与Takeda签署合作协议。韩国Galux与Boehringer Ingelheim合作开发抗体模型,而LabGenius与Sanofi达成合作,进一步显示AI抗体设计正在快速进入产业化阶段。
目前,大多数公司并不是完全从头开始设计抗体,而是基于已有抗体框架,通过生成式模型优化重链和轻链中的氨基酸序列,以改善稳定性、溶解性、免疫原性以及效应功能,例如Fc受体回收或抗体依赖的细胞毒作用。这种基于骨架优化的方法已经能够显著提升抗体的可开发性。
然而,真正困难的部分在于预测抗体与抗原的结合能力。抗体的特异性由六个互补决定区(CDR)决定,而这些环状结构具有高度柔性,可用的高分辨率结构数据仅约一万例,使得精确预测亲和力极具挑战。部分公司已经可以利用机器学习优化已知抗体的CDR区域,但更大的目标是完全从头生成具有纳摩尔甚至皮摩尔亲和力的抗体。
尽管许多AI公司宣称其模型已经可以与实验方法竞争,但缺乏同行评审论文和公开基准,使得这些成果难以验证。Specifica公司科学负责人Andrew Bradbury组织了AIntibody Challenge基准测试,要求模型针对SARS-CoV-2受体结合域设计抗体。来自29家机构的模型结果显示,AI设计抗体的表现仍未明显超过传统展示技术,部分预测抗体甚至无法结合或存在开发风险。
研究人员认为,当前AI抗体设计的进步部分来自更强的计算能力和更大的基础模型。随着GPU算力提升,模型可以学习更通用的原子和分子相互作用规律,从而在数据不足的情况下仍能获得较好性能。另一方面,新的算法架构和与湿实验紧密结合的循环优化,也在推动模型快速提升。
随着公开蛋白序列数据量的爆炸式增长,模型训练数据也越来越丰富,但专家指出,仅靠更多数据并不足以解释性能飞跃,尤其是在CDR环预测等困难问题上。
当前模型已经能够从简单的纳米抗体扩展到更复杂的抗体形式,但随着抗体结构复杂度增加,所需训练数据、实验验证和过滤步骤也大幅增加。未来最具吸引力的目标是双特异或多特异抗体,因为生成式模型有望同时控制多个结合位点,从而减少传统试错过程。
研究人员也在尝试将AI用于更困难的靶点,例如GPCR或动态膜蛋白。这类靶点长期以来难以通过抗体药物靶向,而生成式模型可能提供新的解决方案。
短期内,AI更可能用于加速现有流程,例如筛选展示库结果、缩短亲和力成熟时间或减少开发风险。但长期目标是设计能够直接进入临床开发的全新抗体药物,并降低研发成本。
前制药公司高管Stefan Oschmann认为,这项技术可能改变药物研发成本不断上升的趋势。一旦首个完全由AI设计的生物药成功进入临床,整个行业将迅速转向计算驱动的研发模式。
目前,学术界呼吁更多公开数据和盲测竞赛,以验证模型真实性能。类似CASP对AlphaFold的验证方式,被认为是抗体设计领域未来的关键。
尽管仍存在争议,行业整体情绪依然乐观。越来越多研究人员相信,未来抗体开发将不再依赖大量随机筛选,而是通过计算机直接设计目标分子。正如Baker所说,抗体工程正在从“不断试错”转变为“先设计,再构建”的新时代。
整理 | DrugOne团队
参考资料
Marshall, A. AI turbocharges antibody hunt for binders with drug-like qualities. Nat Biotechnol 44, 334–337 (2026).
https://doi.org/10.1038/s41587-026-03048-w

内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-03-20,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

