Nat. Health | 用AI精准匹配医生与临床试验,提升临床研究效率
Nat. Health | 用AI精准匹配医生与临床试验,提升临床研究效率

DrugAI
发布于 2026-03-30 18:52:06
发布于 2026-03-30 18:52:06
DRUGONE
临床试验中心和研究者的选择过程往往效率低下,导致受试者招募不足、人群代表性差以及高昂的时间成本。研究人员开发了一种名为 DocTr 的跨模态深度学习框架,用于自动匹配临床试验与合适的医生。该模型同时整合医疗索赔数据、临床试验文本信息以及历史入组关系数据,从而在保证匹配准确性的同时兼顾公平性和运营效率。在包含 24,984 名医生和 5,210 项临床试验的大规模数据集上,DocTr 的匹配相似度比现有方法提高约 58%。进一步结合遗传算法优化后,模型能够显著提高种族和族裔公平性,并减少医生同时参与多个试验的冲突,同时还能预测招募成本。该方法有望显著提升临床试验中心选择效率,加速新疗法进入临床。

临床试验是医学进步的重要基础,但试验能否成功,很大程度上取决于试验中心和研究医生的选择。传统的人工选择方式通常依赖经验和有限的信息来源,容易受到地域限制和主观偏差影响,导致招募效率低下。已有研究表明,大量临床试验存在入组不足甚至完全无法招募受试者的情况,同时试验延期会带来巨大的经济损失。
利用人工智能根据医生的患者结构与试验需求进行匹配,是一种有前景的解决方案。与现有研究多关注“患者–试验匹配”不同,本研究聚焦于“医生–试验匹配”,通过选择合适的研究医生来提高整体招募效率。然而,该任务面临多方面挑战,包括数据来源分散、隐私限制、试验文本为非结构化信息,以及匹配结果需要同时满足准确性、公平性和实际运营约束。
为解决这些问题,研究人员提出跨模态深度学习模型 DocTr,通过融合试验文本、患者就诊数据和历史试验参与关系,实现更可靠的临床试验中心推荐。
方法
研究人员构建了一个多源整合数据集,包含临床试验文档、医疗索赔记录、人口统计数据以及医生参与试验的支付记录,并将临床试验中心选择问题建模为排序任务:对于每个试验,模型计算每位医生的匹配得分,并生成推荐列表。
模型由三个核心部分组成。首先,通过自然语言模型对试验摘要和入选标准进行编码,同时利用患者诊断编码统计描述医生的患者群体结构,从而得到语义特征表示。其次,根据历史试验参与关系构建医生–试验异构图,并使用图神经网络提取结构特征。最后,将语义特征与结构特征结合计算匹配得分,并通过遗传算法对推荐结果进行多目标优化,使结果在准确性、公平性和试验竞争程度之间取得平衡。
此外,模型还利用相似试验和相似医生的信息,对试验招募成本和入组人数进行预测,以支持实际决策。
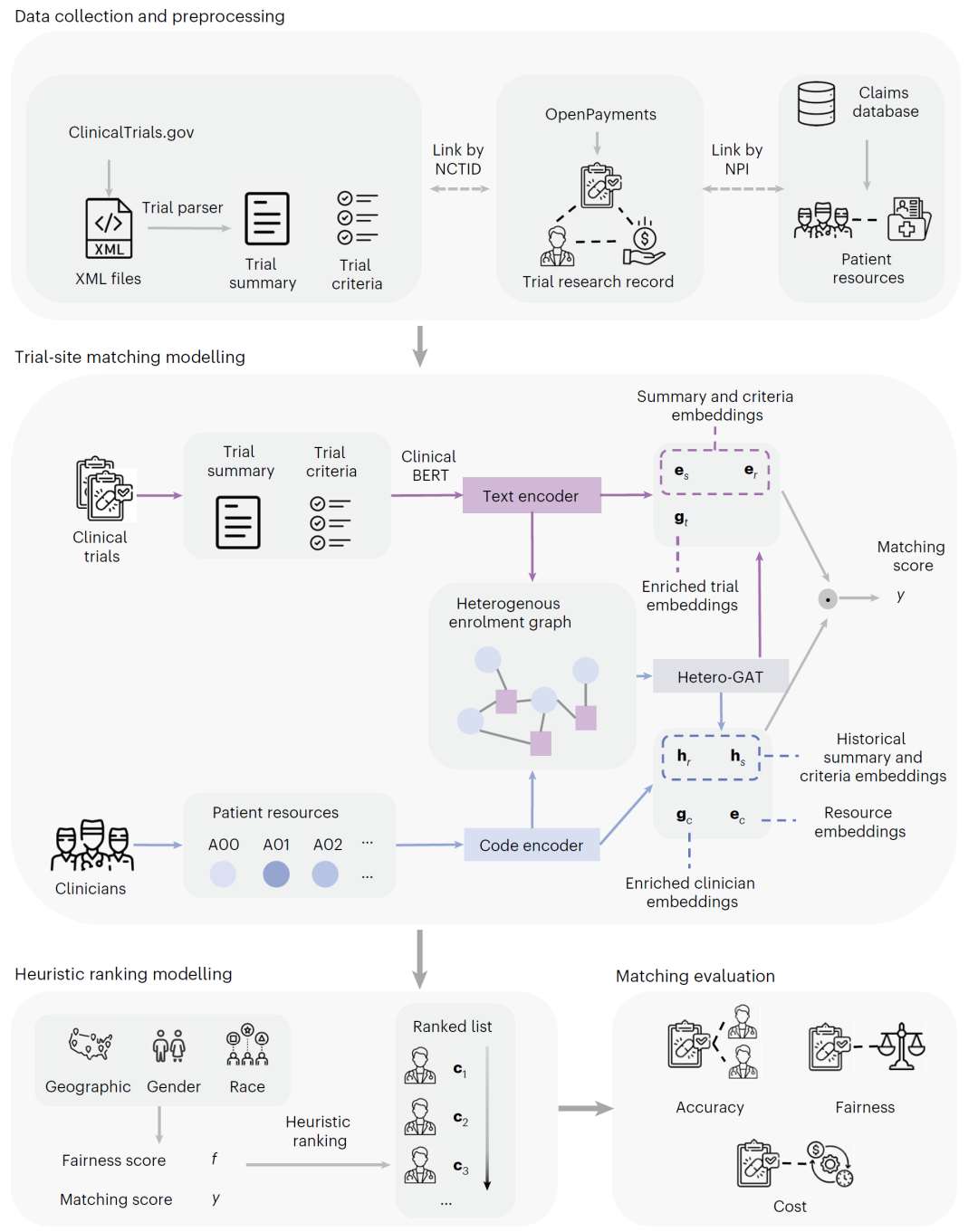
图1: DocTr模型总体框架。
结果
数据集与评价指标
研究人员整合了来自 ClinicalTrials.gov、医疗索赔数据库、人口统计数据以及 OpenPayments 的信息,构建了一个包含数千项临床试验和数万名医生的大规模关联数据集。历史支付记录被用作医生参与试验的真实标签。模型性能通过匹配相似度、公平性熵值以及成本预测准确度等指标进行评估。
新临床试验上的匹配性能
在模拟真实场景的时间划分实验中,测试集包含训练阶段从未见过的新试验和部分新医生。结果显示,DocTr 在所有评价指标上均明显优于现有方法,匹配相似度提升超过 50%。同时,即使在完全未知试验的情况下,模型仍保持稳定性能,说明跨模态表示能够有效捕捉医生与试验之间的潜在关联。
与只使用文本信息或只使用历史关系的模型相比,完整模型表现更好,说明语义信息和结构信息的结合对于推荐至关重要。
公平性与试验竞争控制
临床试验推荐不仅需要准确,还需要保证不同地区、族群和人群的公平参与。研究人员在推荐阶段加入遗传算法,对结果进行多目标优化,使推荐医生在种族、族裔和地理分布上更加均衡。
结果显示,在不降低匹配准确性的情况下,优化后的模型显著提高了公平性指标。同时,每位医生被分配到的同时进行中的试验数量明显减少,接近于零,从而降低实际操作中的冲突,提高试验执行效率。
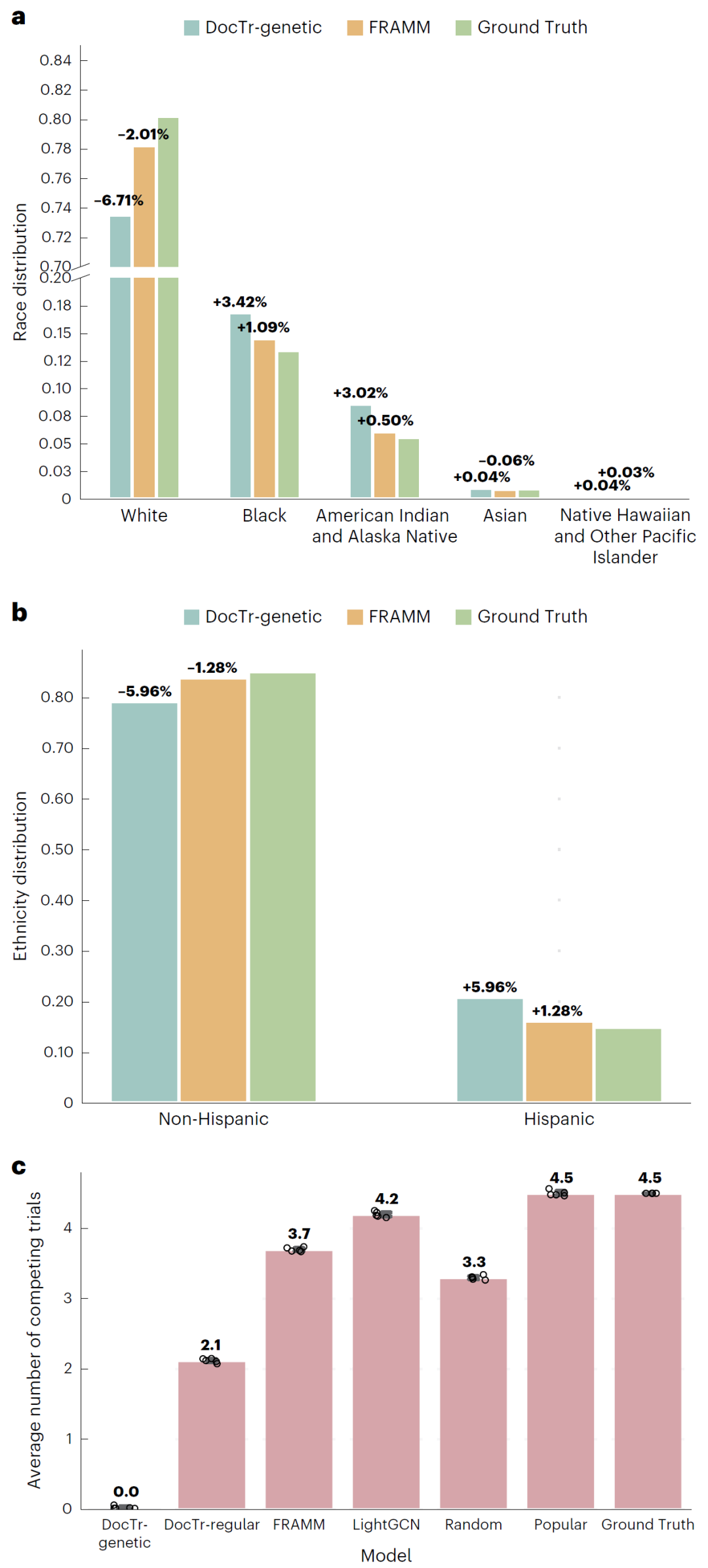
图2:DocTr与基线模型在种族、族裔分布及竞争试验数量方面的比较。
招募成本与入组预测
临床试验规划需要提前估计成本和入组规模。DocTr 利用学习到的嵌入表示,寻找与当前试验最相似的历史试验,从而预测总成本、入组人数以及单个医生的招募费用。
实验结果表明,模型在成本预测方面具有较高一致性,能够较准确地估计试验预算和医生相关费用。这种能力可以帮助研究团队在试验开始前制定更合理的资源分配方案。
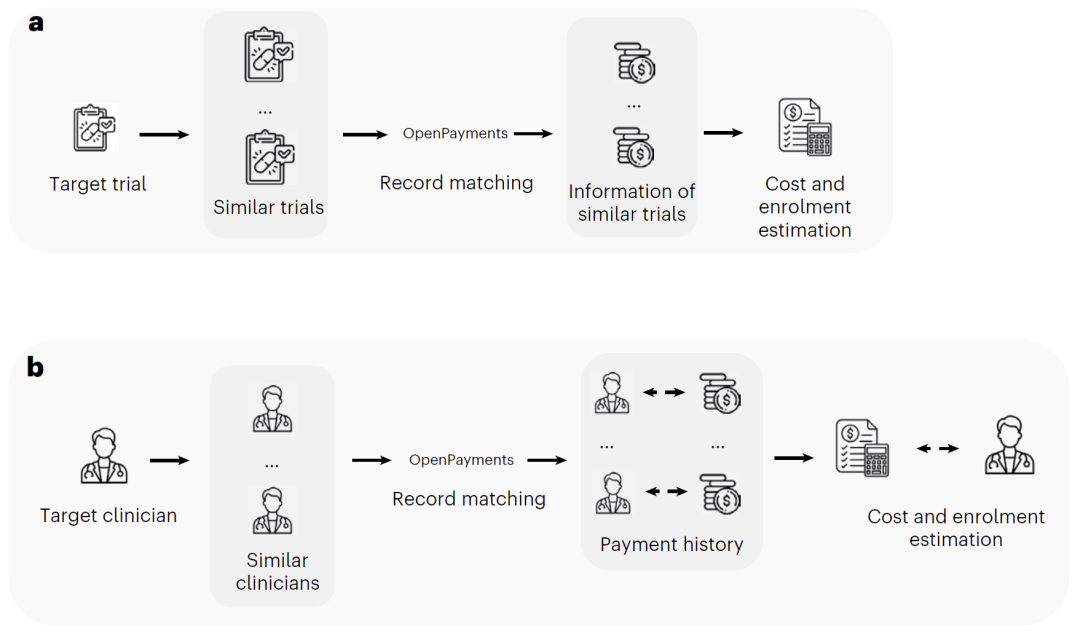
图3:招募成本预测流程。
讨论
本研究提出的 DocTr 模型证明,跨模态深度学习可以显著提升临床试验中心选择的效率和质量。通过整合文本、患者数据和历史关系信息,模型能够准确识别最合适的医生,并在保证公平性的同时减少试验冲突。
研究人员指出,该方法并不是取代人工决策,而是为试验管理者提供数据驱动的候选列表,使其在此基础上结合专家经验进行最终选择。现实中,试验中心的选择还会受到关键意见领袖、机构合作关系等因素影响,这些信息目前尚未完全纳入模型。
研究也存在一定局限。例如,成本数据来源于支付记录,可能无法完全反映真实招募费用;患者人口学信息缺乏,只能用地区统计数据进行近似;数据主要来自美国,因此模型的泛化能力仍需进一步验证。
未来研究可以通过引入更丰富的电子病历、机构信息以及全球多地区数据,构建更全面的临床试验推荐系统,从而进一步提高临床研究的效率和公平性。
整理 | DrugOne团队
参考资料
Gao, J., Xiao, C., Glass, L.M. et al. Matching clinicians with clinical trials using AI. Nat. Health 1, 290–299 (2026).
https://doi.org/10.1038/s44360-026-00073-6

内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-03-24,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

