Nat. Mach. Intell. | 通过语言模型在口袋中生成三维分子结构
Nat. Mach. Intell. | 通过语言模型在口袋中生成三维分子结构

DrugOne
发布于 2024-03-04 13:09:26
发布于 2024-03-04 13:09:26
今天为大家介绍的是来自Bo Huang和Wenbiao Zhou团队的一篇论文。基于序列或图表示的分子生成模型,在基于结构的药物设计领域越来越受到关注。然而,这些模型往往难以捕捉重要的三维(3D)空间交互作用,并常常生成不理想的分子结构。为了解决这些挑战,作者提出了一种新方法——Lingo3DMol,这是一种基于口袋的3D分子生成方法,结合了语言模型和几何深度学习技术。

基于结构的药物设计,即设计能特定结合目标蛋白的分子,是药物发现中的一个基础且具挑战性的任务。使用人工智能进行全新分子的生成,近来作为药物发现工具受到了关注。早期的分子生成模型依赖于分子字符串表示或图形表示。然而,这些表示方法忽视了三维(3D)空间交互,使得它们在目标导向的分子生成中表现不佳。3D蛋白-配体复合体结构数据的增加和几何深度学习的进步,为人工智能算法直接设计具有3D结合位向的分子铺平了道路。一些研究提出将口袋和分子表示为3D图,并使用图神经网络(GNN)进行编码和解码。这些GNN模型使用自回归生成过程,将分子图线性化为一系列采样决策。尽管这些方法可以生成具有3D构象的分子,但它们也存在一些共同的缺点:(1)生成的分子常含有问题性的、非药物样或合成上不可获得的亚结构;(2)问题性拓扑:生成的分子常含有过多或根本没有环结构。自回归采样方法有其固有的局限性。它在分子生成的初期容易陷入局部最优,并可能累积每个采样步骤引入的错误。例如,虽然模型可以准确地定位第n个原子以创建苯环,但由于上下文信息不足,初始原子的准确放置通常是有问题的,导致生成不切实际的片段。此外,还有一些基于其他技术路线的3D分子生成方法,如基于扩散模型的方法。代表性方法是TargetDiff,它使用基于图的扩散模型进行非自回归分子生成。尽管它努力避免自回归方法的问题,但仍然生成了相当比例的不理想结构。这个问题可能是由于模型对分子拓扑的相对弱感知所致。因此,尽管TargetDiff在早期模型的基础上取得了改进,但在药物相似性量化估计(QED)和合成可达性评分(SAS)等指标上仍有提升空间。
模型部分
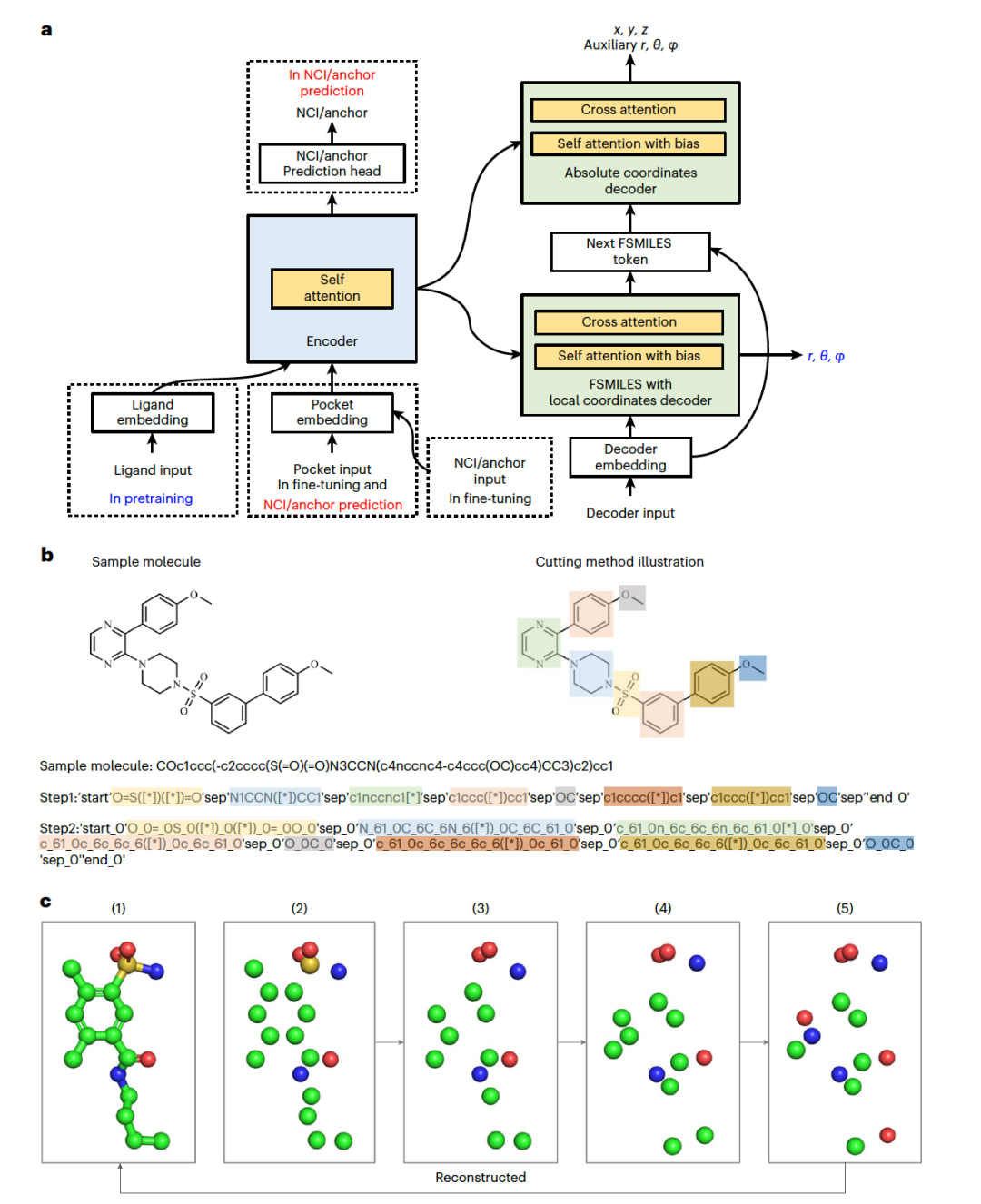
图 1
图1a-c展示了整体架构和预训练策略。在作者的评估中,对Lingo3DMol与基线方法进行了比较分析。作者从三个主要角度评估生成的分子:分子几何、分子属性分布和在口袋中的结合模式。
分子几何
生成分子的键长分布是使用一种类似于TargetDiff研究中使用的方法来评估的。具体来说,作者为该研究中测试的三个模型各生成了大约10,000个分子。这些分子是为CrossDocked2020数据集中的100个靶点生成的。然后,作者将生成分子的键长分布与参考分子的键长分布进行了比较,这些参考分子包括从CrossDocked2020数据集中选取的100个配体,与TargetDiff研究中使用的相同。作者的模型和基准模型都显示出良好的性能,如同参考分子一样,表现出相似的平均键长。对于其他几何相关问题如环的大小分布作者的模型也比基线模型要好很多。
分子性质和结合模式
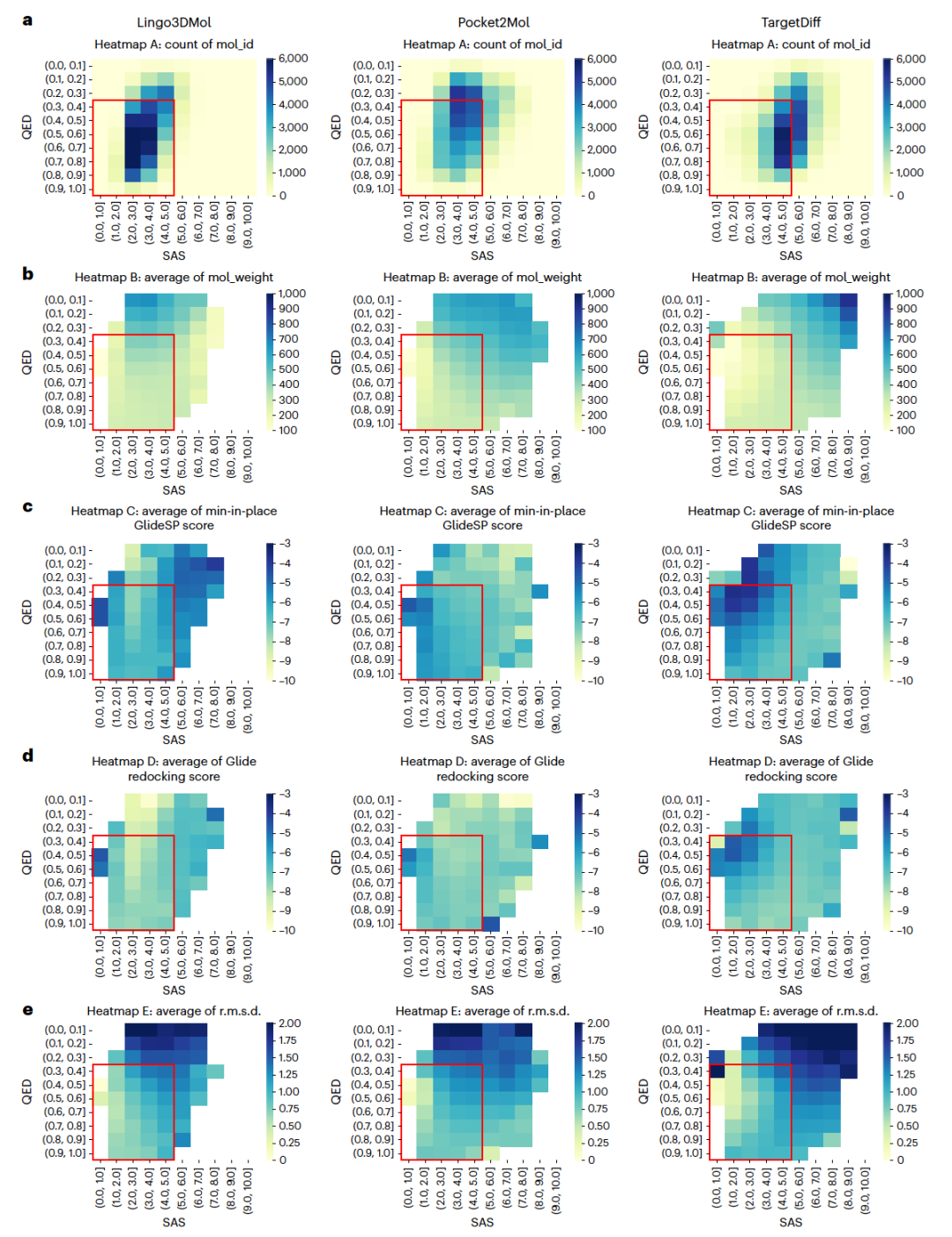
图 2
作者使用DUD-E中的靶点来测试模型。关于结合模型评估工具,作者使用Glide。关于结合模型评估的评价指标,有三个选项: min-in-place GlideSP分数、in-place GlideSP分数和GlideSP重新对接分数。min-in-place GlideSP分数是通过使用“min-in-place”对接方法获得的,在该方法中,配体结构在评分前在受体的力场中进行基于力场的能量最小化。它要求配体相对于受体的初始放置非常准确。in-place GlideSP分数是通过使用“in-place”对接方法生成的,直接使用输入的配体坐标进行评分,不涉及任何对接或能量最小化。GlideSP重新对接分数涉及将生成的分子对接到口袋中,包括探索配体结合构象和初始放置。在评估结合模型的三个对接相关指标中,作者主张使用min-in-place GlideSP分数。min-in-place GlideSP GlideSP分数尊重模型生成的初始结合模型,并通过基于力场的调整对其进行优化,以获得稳健的评分。仅使用GlideSP重新对接分数,而不考虑min-in-place GlideSP分数,将与3D生成的目标相矛盾,因为它忽略了原始位向。
在进行结合模式评估之前,作者强调检查分子性质分布的重要性。在计算GlideSP分数之前排除药物相似性不足或合成可达性有限的分子变得至关重要。为了进一步调查这一筛选标准在更大规模上的重要性,作者对生成分子的各种关键性质分布进行了深入分析,使用热图展示(图2a-e)。重要的是要注意,如图2c所示,具有良好最小现场Glide分数(较低分数)的分子,大多数位于Pocket2Mol和TargetDiff的药物样区域之外,这一区域由红框标示。为了定义药物样区域,作者考虑了QED值在0.3或更高以及SAS值在5或更低的分子,这覆盖了DrugBank中超过80%的分子。与基准模型不同,Lingo3DMol显示出不同的模式。具体来说,Lingo3DMol倾向于生成具有相对良好min-in-place GlideSP分数的药物样分子。
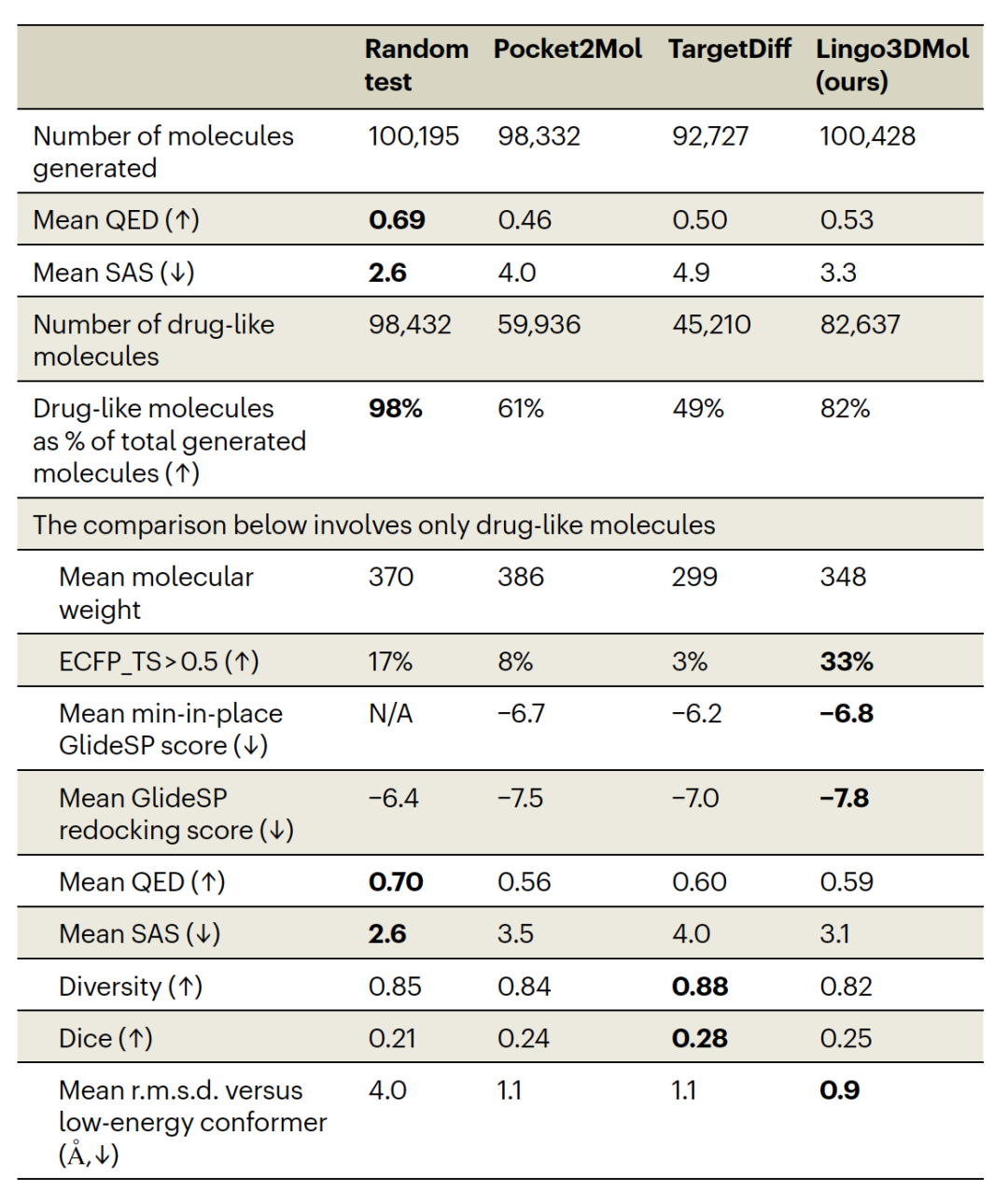
表 1
在结合模式评估方面,基于上述分析,结果在表1中展示。尽管平均QED和SAS值并没有显著区分作者的模型和基线,但通过结合QED和SAS确定的药物样分子的百分比表明了作者模型的优越性。此外,除了生成药物样分子之外,有效的分子生成模型还应能生成活性化合物。由于在现实世界中合成所有生成的分子是不切实际的,因此一种替代方法是评估模型是否能复制已知的活性化合物或生成与已知活性化合物高度相似的分子。为了评估这一点,作者引入了指标“ECFP_TS > 0.5”,代表具有超过0.5 Tanimoto相似度(与活性化合物的ECFP相比)的靶点中生成化合物的百分比。在三个模型生成的药物样分子中,作者的模型对33%的靶点产生了类似于活性化合物的化合物,超过了Pocket2Mol的8%和TargetDiff的3%。此外,对于3D分子生成模型来说,生成具有靶点口袋中有利结合的分子至关重要。这种评估可以从两个角度进行:与口袋的结合模式以及配体的能量,这两者通常与良好的结合亲和力相关。作者使用min-in-place GlideSP分数来评估口袋相互作用,并使用均方根偏差(r.m.s.d.)与低能量构象相比来反映配体的应力能量。尽管r.m.s.d.与低能量构象的指标并没有直接以kcal mol−1的单位量化应力能量,但它提供了有价值的信息,显示生成的构象在整体几何形状上与低能量构象的相似度。这个指标作为评估配体应力能量的代理。生成的构象与ConfGen中最低能量的前20个构象进行了比较。Lingo3DMol在GlideSP分数和r.m.s.d.方面超越了基准线,表明作者模型生成的构象相对于基准模型的高质量。
编译 | 曾全晨
审稿 | 王建民
参考资料
Feng, W., Wang, L., Lin, Z. et al. Generation of 3D molecules in pockets via a language model. Nat Mach Intell 6, 62–73 (2024).
https://doi.org/10.1038/s42256-023-00775-6
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2024-03-03,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

